Foramen oval permeable y aneurisma del septo interauricular
Introducción
El foramen oval permeable (FOP) es la persistencia tras el nacimiento del fo-ramen oval, una estructura fisiológica, necesaria durante la etapa fetal para la oxigenación de la sangre, que permite la comunicación entre aurícula derecha primitiva y aurícula izquierda. En la mayoría de los sujetos, en el momento en que se inicia la circulación pulmonar esta estructura tiende a cerrarse, mientras que en aproximadamente un 25 % de la población este cierre es incompleto y persiste la comunicación interauricular.
En los últimos años el FOP esta siendo motivo de numerosos estudios al con-siderarse que su presencia puede estar relacionada con el ictus isquémico y la migraña con aura.
La primera documentación en la que se relaciona la presencia de un FOP con fenómenos de embolismo paradójico data del 1877 en un texto de Julius Coh-neim.
Etiología
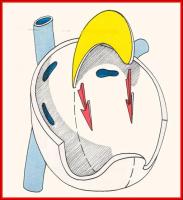
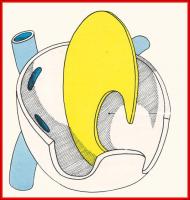
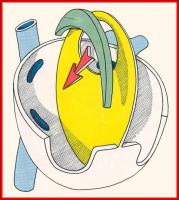
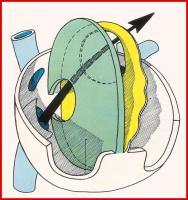
Al final de la cuarta semana de gestación se forma, en el techo de la aurícula común del corazón fetal, una cresta falciforme que desciende en dirección a las almohadillas endocárdicas en el canal auriculoventricular, esta cresta supone la primera porción del septum primum. El orificio que queda entre el borde inferior del septum primum y las almohadillas endocárdicas recibe el nombre de ostium primum. (Ver Figuras 1 y 2 jpg)
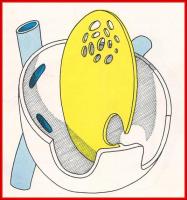
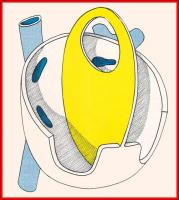
Del mismo modo desde las almohadillas endocárdicas aparecen prolongacio-nes que siguen el borde del septum primum y cierran gradualmente el ostium primum. Antes de completarse el cierre completo, en la parte superior del sep-tum primum se produce por muerte celular un nuevo orificio que recibe el nom-bre de ostium secundum que permite la comunicación entre la aurícula primitiva derecha y la izquierda. (Ver Figuras 3, 4 y 5 jpg)
Mas adelante, desde el techo de la aurícula primitiva derecha, aparece un nue-vo pliegue que no llega a separar por completo la cavidad auricular y que se denomina septum secundum. Este pliegue se superpone al ostium secundum pero no llega a ocluirlo por completo permitiendo la comunicación entre las dos aurículas. El orificio que queda entre el septum secundum y el septum primum es lo que llamamos foramen oval. (Ver Figuras 6 y 7 jpg)
El foramen oval consiste en una hendidura oblicua y alargada por la cual pasa sangre de la aurícula derecha hacia el lado izquierdo imprescindible para que el feto reciba la sangre oxigenada procedente de la madre.
Después del nacimiento, al iniciarse la circulación pulmonar y aumentar la pre-sión en la aurícula izquierda, el septum primum y el septum secundum tienden a fusionarse obliterando el foramen oval y produciendo la separación completa entre aurícula derecha e izquierda.
Como hemos apuntado anteriormente, hasta en un 25 % de la población este cierre es incompleto dándose lo que conocemos como FOP. El motivo por el que esto ocurre no se conoce, pudiendo estar implicados factores genéticos.
Epidemiología
En un estudio autópsico realizado en 1984, se estudiaron 965 corazones de individuos normales con un rango de edad que abarcaba desde 1-100 años. Se observó que la incidencia media de FOP en la población general era del 27%.
No existieron diferencias en cuanto al tamaño del FOP entre hombres y muje-res. Sí que se objetivó, sin embargo, que con el incremento de edad descendía la incidencia de FOP, y así en las primeras tres décadas era del 34.3%, entre la cuarta y la octava del 25.4%, y entre la novena y décima del 20.2%.
De forma contraria el tamaño del FOP tendía a hacerse mayor con el paso del tiempo, pasando de 3.4 mm en las primera década de vida, a 5.8 mm en la dé-cima.
FORAMEN OVAL PERMEABLE, ANEURISMA DEL SEPTO AURICULAR E ICTUS
Llamamos ictus criptogénicos a aquellos en los que no se identifica una causa responsable del mismo. Suponen hasta el 40 % del total de ictus isquémicos, esta proporción es mayor en pacientes jóvenes (<55 años). En los últimos años la presencia de un FOP, asociado o no a un ANEURISMA DEL SEPTO AURICULAR (ASA), se esta convirtiendo en una de las causas potenciales mas fre-cuentemente detectadas en el estudio etiológico de ictus criptogénicos. El ASA es la presencia de un remanente de tejido del septum interauricular situado en la zona del foramen oval. Se considera que esta presente cuando su vértice protruye hacia alguna de las aurículas al menos 10-15 mm. Su asociación al FOP se cree que confiere un mayor riesgo de ictus isquémico por aumento de la turbulencia del flujo sanguíneo que pasa a través del FOP.
El interés por intentar encontrar la asociación entre ictus isquémico y FOP sur-gió a partir de un estudio francés realizado en 1988 donde por medio de la eco-cardiografía transtorácica y el uso de contraste salino se demostró una preva-lencia superior de FOP en pacientes con un ictus criptogénico (54%) con res-pecto a la población control (15%).
En un metanálisis realizado por Overell en el año 2000 de los distintos estudios retrospectivos que han intentado establecer una relación entre FOP e ictus is-quémico, se puso de manifiesto que la presencia de un FOP junto a un ASA se asocia de forma significativa con ictus isquémicos en pacientes menores de 55 años mientras que en los mayores de 55 años no se podía establecer esta asociación.
Podemos decir, por tanto, que la asociación entre FOP e ictus isquémico es evidente, sin embargo la relevancia clínica del FOP como factor de riesgo inde-pendiente de ictus continua siendo controvertida en parte debido a los errores en el diseño de los trabajos publicados hasta ahora.
Son varios los estudios prospectivos que han tratado de arrojar un poco de luz sobre el tema con resultados distintos. Si se ha confirmado una mayor preva-lencia de FOP y ASA en pacientes con ictus isquémico criptogénico que pre-sentan recurrencias.
Patogénesis
El mecanismo mas extendido por el cual la presencia de un FOP podría estar implicado en la etiopatogénesis de un ictus es el de la embolia paradójica. Trombos procedentes del territorio vascular venoso pasarían desde la aurícula derecha a la aurícula izquierda fa-vorecidos por un aumento de la presión en cavidades derechas, como ocurre durante la maniobra de Valsalva, pasando a la circulación arterial cerebral y provocando el ictus isquémico. Para poder decir que se ha producido un embo-lismo paradójico es necesario que se exista un embolismo arterial y que coexis-tan trombosis venosa, comunicación interauricular o shunt derecha-izquierda; y aunque existen casos bien documentados, no siempre se encuentre una fuente de trombosis venosa. En alguno de los estudios realizados al respecto (estudio PELVIS) se ha sugerido que la fuente embolica podría estar a nivel pélvico. Pe-se a todo, la ausencia de factores que apoyen dicho mecanismo en los ictus asociados a FOP como serían antecedentes de trombosis venosa profunda, criterios clínicos o ecocardiográficos de hipertensión pulmonar y especialmente antecedentes de maniobras de Valsalva que favorezcan el shunt derecha-izquierda obliga a plantearse otros mecanismos etiopatogénicos.
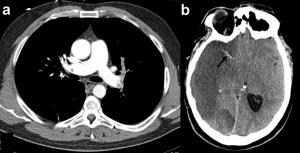
Figura 8. Varón de 46 años que tras periodo de inmovilización involuntaria de 24 horas, presenta cuadro súbito, tras levantarse e iniciar el aseo, de disminu-ción del nivel de conciencia, hipotensión y desaturación de oxígeno al 70%. Posteriormente es intubado y se realiza angio-TC torácico que ofrece signos de tromboembolismo pulmonar (TEP) masivo bilateral (a). Al intentar la extubación a las 48 horas persistía bajo nivel de conciencia con ausencia de respuesta a estímulos. Se realizó TC craneal (b) que mostró un infarto masivo en el territo-rio de la arteria cerebral media y posterior derechas, con signo de la cuerda en la arteria cerebral media (flecha). En doppler transcraneal realizado se detectó patrón de shunt derecha izquierda, probablemente secundario a un foramen oval permeable que permitió la aparición de un embolismo paradójico como mecanismo del infarto cerebral.
También se ha sugerido que los pacientes con FOP e ictus criptogénicos presenten estados procoagulantes con mayor frecuencia que la población general. Existe algún trabajo sobre el tema donde no se ha confirmado esta hipótesis. Si se ha visto como los pacientes que han sufrido un ictus criptogénico tienen una ma-yor incidencia de estados procoagulantes, pero independientemente de si tie-nen o no FOP.
Si bien es cierto que el embolismo paradójico es una hipótesis atractiva, no ha podido confirmarse. Podríamos plantearnos otras posibilidades como son si ciertos estados procoagulantes no los sabemos identificar con los medios ac-tuales o si los ictus isquémicos son secundarios a estados procoagulantes transtorios como ocurriría en el síndrome de la clase turista, que debido a la inmovilidad durante horas que existe en los viajes de largo recorrido se favore-ce la formación de trombosis venosas, la mayoría de ellas asintomáticos y por tanto infradiagnosticadas. En este contexto se encuadra el ictus de la clase tu-rista (Belvís 2005).
Otras hipótesis etiopatogénicas son: la organización del trombo en el mismo orificio anatómico que constituye el FOP o la formación de trombos en la aurícula izquierda como consecuencia de arritmias auriculares sobre todo en aque-llos pacientes que asocian ASA, basado en un estudio en el que pacientes con defectos del septo auricular tenían mayor incidencia de fibrilación auricular.
Algunos autores sugieren que son solo algunos FOP con determinadas carac-terísticas, y no todos, los que se asocian con un aumento del riesgo de sufrir ictus isquémicos. Y así hacen referencia a un moderado-gran tamaño (>4mm), shunt derecha-izquierda masivo, aumento de la movilidad del septo auricular por asociación de ASA…
Diagnostico
- Ecocardiografía transesofágica (ETE): Ha sido considerado el gold standard para la detección de FOP con mucho mayor rendimiento que la ecocardiografía transtorácica. Nos permite evaluar no solo la presencia de FOP sino también su tamaño y si esta asociado o no a ASA. Para la detección de shunt D-I se utiliza el test del paso de burbujas que consiste en la infusión de un contraste de suero salino fisiológico agitado a través de una vía venosa periférica detectando su paso a través del FOP por imagen ecográfica. Los inconvenientes que presenta esta prueba es que es invasiva, requiere la colaboración del paciente y no esta exenta de riesgos como broncoespasmos, hipoxia, arrítmias, traumas en aparato digestivo con sangrados secundarios. En un reciente estudio prospectivo realizado por cardiólogos y neurólogos, que incluye a 134 pacientes, los cuales fueron seleccionados por que habían padecido un ictus criptogénico o migrañas, se compara la eficacia de las tres técnicas que se emplean en la práctica clínica en el diagnóstico del foramen oval permeable. El ecocardiograma transtorácico, el ecocardiograma transesofágico y el doppler transcraneal, mostraron unas cifras de sensibilidad y especificidad para su detección, del 100%/100%; 86%/100%, y 97%/98% respectivamente. Asimismo, la cuantificación de la intensidad del shunt derecha-izquierda era mejor estimada por ecocardiografía transtorácica que por ecocardiografía transesofágica. La mejor capacidad para la visualización de las microburbujas, gracias a la imagen armónica, disponible en los equipos actuales de ecocardiografía transtorácica, explica su mayor capacidad diagnóstica. La presencia de aneurisma del septo interauricular, fue también fácilmente detectable con ecocardiograma transtorácico. Dados estos resultados, los autores consideran que el ecocardiograma transesofágico en este contexto puede ser reservado para aquellos pacientes con mala ventana acústica, y en los que se vaya a planificar el cierre del foramen oval (González-Alujas 2011).
- Doppler transcraneal (DTC). Nos permite detectar con una alta sensibilidad la presencia de shunt derecha-izquierda (mayor que con ETE). Monitorizamos una de las arterias cerebrales medias a través de la ventana temporal (zona donde el hueso del cráneo es más delgado). Posteriormente agitamos suero salino fisiológico, con el fin de formar microburbujas, y lo administramos por vía venosa periférica, preferiblemente en flexura del brazo. Si hubiese paso de burbujas a través de un hipotético FOP se detectarían señales de alta densidad ecográfica por medio del DTC. La prueba debe hacerse tanto en si-tuación basal como tras maniobra de Valsalva, que como hemos dicho anteriormente favorece el paso de burbujas a través del FOP. Existen distintos pa-trones ecográficos que nos permiten relacionar la cantidad de burbujas que pasan a través del FOP con su tamaño y así tenemos que menos de 10 seña-les supondrían un shunt D-I leve y sugieren un tamaño de FOP pequeño; 10-25 señales un shunt moderado y un tamaño medio; y por encima de 25 señales se traduciría en un shunt masivo, con dos posibles patrones ducha o cortina, que sugieren un tamaño grande. (Ver Patrones 1 y 2 jpg). La principal ventaja de esta prueba es que no es invasiva. Tiene el inconveniente de que hasta un 20 % de la población no tienen ventana ósea temporal, es decir, que el hueso a este nivel sea excesivamente grueso.
- Ecocardiograma transtorácico (ETT), es mucho menos preciso que el ETE para el diagnostico de FOP, si bien aumenta su rendimiento si se realiza el test del paso de burbujas de suero salino fisiológico a través de vena periféri-ca. Queda destinado a aquellas situaciones en las que no se pueda realizar un ETE.
La recomendación de cara al algoritmo diagnostico de un hipotético FOP sería inicialmente realizar un DTC (dada su alta sensibilidad) y si muestra la presen-cia de un Shunt D-I confirmar este hallazgo mediante ETE y así explorar la po-sible asociación con ASA y las características morfológicas del FOP.
Tratamiento
Hasta hoy no se han llevado a cabo estudios aleatorizados específicamente diseñados para evaluar las distintas posibilidades terapéuticas utilizadas en la prevención secundaria del ictus asociado a FOP con o ASA. En el estudio CODICIA no se han encontrado que haya una mayor tasa de recurrencia de ictus criptogénico en pacientes menores de 55 años con la presencia de ASA aso-ciado, ni tampoco con la presencia de shunt masivo. Se ha visto también en este estudio que la tasa de recurrencias en este grupo es baja, y suelen ser ic-tus menos severos que los de los pacientes con ictus sin FOP o asociados a la presencia de factores de riesgo vascular, en base a un menor volumen de infar-to y de discapacidad funcional (Serena 2008).
Tratamiento medico
Con respecto al tratamiento médico, se han comunicado resultados contradicto-rios de diferentes estudios que comparan AAS y warfarina. Mientras que en al-gunos parece que la warfarina obtiene una tasa de recurrencias inferior al AAS, estos resultados no han podido confirmarse y en otros estudios no se han en-contrado diferencias significativas en la reducción de recurrencias entre uno y otro grupo, pero sí un discreto aumento de las complicaciones hemorrágicas leves en los pacientes tratados con warfarina.
Algunos autores postulan que el tratamiento debería elegirse en función de las características morfológicas del FOP y si esta asociado o no a ASA, dando por hecho el mayor riesgo de recurrencia en estos últimos por el mayor riesgo de formación de trombos in situ dado el aumento de la turbulencia del flujo san-guíneo que produce dicho ASA.
Las actuales recomendaciones en cuanto a la prevención secundaria del ictus asociado al FOP están basadas por tanto, más en la opinión de expertos, que en resultados concluyentes de estudios científicos. Habrá pues que esperar los resultados de estudios randomizados que comparen las distintas modalidades terapéuticas.
FOP AISLADO:
El tratamiento antiagregante con AAS a dosis entre 80-325 mg cada 24 horas sería el tratamiento de elección.
En aquellos pacientes con FOP y una trombosis venosa profunda documenta-da, tromboembolismo pulmonar y/o estados de hipercoagulabilidad, el trata-miento de elección seria la anticoagulación en rango de INR 2-3, durante el tiempo indicado por el tromboembolismo venoso y después continuar la pre-vención secundaria con antiagregación.
Si existe recurrencia a pesar del tratamiento médico con antiagregación o anti-coagulación se debería plantear el cierre percutáneo del FOP.
FOP ASOCIADO A ASA
Las recomendaciones son las mismas que en el caso de FOP aislado, aunque algunos autores, amparándose en el resultado de alguno de los estudios reali-zados y en el supuesto mayor riesgo de trombosis in situ en estos pacientes, proponen la anticoagulación crónica como primera opción terapéutica.
ASA AISLADO
El tratamiento antiagregante con AAS a dosis entre 80-325 mg cada 24 horas sería el tratamiento de elección.
En aquellos pacientes con ASA y una trombosis venosa profunda documenta-da, tromboembolismo pulmonar y/o estados de hipercoagulabilidad, el tratamiento de elección seria la anticoagulación en rango de INR 2-3, durante el tiempo indicado por el tromboembolismo venoso y después continuar la pre-vención secundaria con antiagregación.
En casos de recurrencia a pesar del tratamiento medico se puede considerar la reparación quirúrgica del ASA como opción terapéutica.
Tratamiento quirúrgico:
El cierre percutáneo es una posibilidad todavía controvertida, pero que ha demostrado ser segura y al menos tan eficaz como el tratamiento médico en la reducción de recurrencias, por lo que se considera una indicación de tratamiento en los pacientes con embolismos recurrentes asociadas a foramen oval permeable.
En marzo de 2012 se han publicado los resultados del estudio CLOSURE en la revista NEJM. En este estudio se evaluaba el cierre del FOP mediante un procedimiento percutáneo frente a terapia médica en un grupo de más de 900 pacientes jóvenes (edades entre 18 y 60 años) con un ictus o accidente isquémico transitorio de causa desconocida salvo por el hallazgo del FOP. Los resultados no han mostrado diferencias entre ambas ramas terapéuticas con una tasa de ictus en los dos años de seguimiento de 2,9 % en la rama quirúrgica frente al 3,1 % de la rama médica (p=0,79). No obstante, el procedimiento percutáneo fue seguro sin complicaciones relevantes (Furlan et al, 2012). Los hallazgos de este estudio se han discutido en el blog de Neurowikia.
Diversos trabajos sugieren que la oclusión percutánea del FOP constituiría la mejor opción terapéutica en el ictus criptogénico asociado a FOP, sin embargo la utilización de estos sistemas no esta exenta de riesgos, y aunque son efica-ces en la oclusión del FOP sus efectos biológicos no son, por el momento, bien conocidos. Así se ha observado que alguno de los materiales utilizados en estos sistemas induce una activación significativa, tanto de la agregación plaque-taria como del sistema de coagulación. De hecho un porcentaje nada desdeña-ble de pacientes que alcanza el 8 % sufren un evento tromboembólico en el primer año tras la oclusión percutánea del FOP, la mitad de los cuales se pro-duce en el primer mes tras la intervención. Este hecho sugiere una clara rela-ción causa-efecto que podría estar justificada por su efecto protrombótico, la persistencia del FOP, la aparición de fibrilación auricular que se asocia en un 10% de los pacientes tras la implantación del sistema de oclusión o la combi-nación de estos factores.
El cierre percutáneo del FOP, aunque prometedor, a espera de resultados mas concluyentes, no deja de ser un procedimiento invasivo no exento de complicaciones (hemorragias intraquirúrgicas, embolismo pulmonar, ruptura del sistema de oclusión, embolización del mismo, hematomas femorales, fístulas…); y tras el cual no tenemos definido el manejo terapéutico ¿Se debe iniciar tratamiento anticoagulante durante unos meses (3-6 meses) por el ya citado aumento del riesgo protrombótico?¿Debe ser tratamiento antiagregante?¿Y tras este tiempo se suspende la prevención secundaria de ictus considerando que el problema esta resuelto o se mantiene algún tipo de tratamiento de forma crónica por el hecho de haber sufrido un ictus criptogénico?
Para contestar estas preguntas se debe esperar a los resultados de los distin-tos estudios aleatorizados actualmente en marcha, que comparan la oclusión percutánea frente al tratamiento medico (PC trial utilizando Amplatzer en Euro-pa, Canada y Australia; CLOSURE con Cardioseal; RESPECT con Amplatzer; y CARDIA con PFO-star en EEUU).
[Prevención secundaria jpg]
Tabla prevención secundaria. FOP: Foramen oval permeable, ASA: Aneurisma del septo interauricular. TEP: Tromboembolismo pulmonar, TVP: Trombosis ve-nosa profunda. AAS: Ácido acetil salicílico.
FORAMEN OVAL PERMEABLE Y MIGRAÑA
Patogenia
Se desconoce el mecanismo por el cual la presencia de un FOP puede relacio-nare con la migraña. Lo que si ha objetivado es que si la presencia de FOP es del 25% entre la población general, en pacientes con migraña con aura ese porcentaje asciende al 67%.
Algunos autores proponen que el paso de sustancias vasoactivas (serotonina, noradrenalina...), que normalmente son metabolizadas a nivel pulmonar, a tra-vés del FOP pasan directamente en la circulación arterial cerebral y provocan una activación plaquetaria o ejercen su acción sobre la vasculatura cerebral y de este modo inducen la crisis de migraña mediante la activación de la depre-sión cortical propagada o por algún otro mecanismo aun no aclarado. Este me-canismo además explicaría el porque pacientes con migraña con aura presen-tan un mayor riesgo de Ictus isquémico evidenciado por una mayor incidencia de lesiones isquémicas silentes en la RMN cerebral.
Otras teorías hablan sin más de una asociación genética en pacientes con mi-graña con aura y FOP.
Tratamiento
Hay autores que sugieren que el cierre percutáneo de un shunt derecha-izquierda podría ser una medida terapéutica mas a la ya existentes en el trata-miento preventivo de la migraña con y sin aura. Esta hipótesis esta basada en el resultado de estudios que carecen de un diseño adecuado o de un segui-miento a largo plazo de los enfermos.
El estudio MIST fue un estudio prospectivo, doble ciego, randomizado, contro-lado y multicéntrico cuyo principal objetivo era comparar la eficacia del cierre percutáneo de FOP en pacientes con migraña con aura refractarios al trata-miento con al menos 2 preventivos diferentes frente al tratamiento medico con-vencional. Los resultados fueron que tras 6 meses de seguimiento no existían diferencias entre los grupos sometidos al cierre del FOP y los que no lo hicie-ron en cuanto a la curación de la cefalea que se estableció como principal obej-tivo de este estudio.
Existen otros estudios en marcha como son el PREMIUM (que compara la efi-cacia del cierre percutáneo del FOP y tratamiento medico, frente a únicamente tratamiento medico) y el MIST II.
A la espera de los resultados de estos últimos actualmente el cierre percutáneo del FOP no esta recomendado como tratamiento para la migraña con o sin au-ra.
BIBLIOGRAFIA
• Anzola GP, Magoni M, Guindani M, Rozzini L, Dalla Volta G (1999). Potential source of cerebral embolism in migraine with aura: a transcranial Doppler study. Neurology. 52(8):1622-5.
• Belvís R, Masjuan J, García-Barragán N, Cocho D, Martí-Fàbregas J, Santamaría A, Leta RG, Martínez-Castrillo JC, Fernández-Ruiz LC, Gilo F, Martí-Vilalta JL (2005). Stroke and pulmonary thromboembolism after a long flight. Eur J Neurol. Sep;12(9):732-4.
• Fuentes B, Díez Tejedor E,Gil Núñez A, Gil Peralta A, Matías Guiu J (2006). Guia para el tratamiento preventivo de la isquemia cerebral. Guia para el diagnostico y tratamiento del ictus de la Sociedad Es-pañola de Neurologia. Editado por Prous Science Provenza. Barce-lona.
* Furlan, A. J., Reisman, M., Massaro, J., Mauri, L., Adams, H., Albers, G. W., Felberg, R., et al. (2012). Closure or medical therapy for cryptogenic stroke with patent foramen ovale. The New England Journal of Medicine, 366(11), 991-999. doi:10.1056/NEJMoa1009639
. González-Alujas T, Evangelista A, Santamarina E, Rubiera M, Gómez-Bosch Z,
Molina C, Alvarez-Sabín et al (2011). Diagnosis and quantification of patent foramen ovale. Which is the reference technique? Simultaneous study with transcranial Doppler, transthoracic and transesophageal echocardiography. Rev Esp Cardiol. Feb;64(2):133-9.
• Hagen PT, Scholz DG, Edwards WD (1984). Incidence and size of patent foramen ovale during the first 10 decades of life: an autopsy study of 965 normal hearts. Mayo Clin Proc. 59(1):17-20.
• Homma S, Di Tullio MR, Sacco RL, Mihalatos D, Li Mandri G, Mohr JP(1994). Characteristics of patent foramen ovale associated with cryptogenic stroke. A biplane transesophageal echocardiographic study. Stroke. 25(3):582-6.
• J. M. Ramírez-Moreno , I. Casado-Naranjo , M. Gómez , J. C. Portilla , M. Caballero , A. Serrano , M. J. Ojalvo , A. Falcón , D. Tena-Mora , M. Calle (2008). Migraña con aura y foramen oval permeable. ¿Una entidad clínica diferente? Neurología. 23(8):475-542
• Kimmelstiel C, Gange C, Thaler D (2007). Is patent foramen ovale closure effective in reducing migraine symptoms? A controlled study. Catheter Cardiovasc Interv. 69(5):740-6.
• Lippmann H, Rafferty T (1993). Patent foramen ovale and paradoxical embolization: a historical perspective. Yale J Biol Med.66(1):11-7.
• Markandaya M, Gatewood R. Medlink of Neurology. Patent foramen ovale. http://www.medlink.com. Marzo 2009.
• Messe SR, Schwartz RS, Perloff JK. Treatment of atrial septal abnormalities (PFO, ASD, and ASA) for prevention of recurrent stroke in adults. In: UpToDate, Rose, BD (Ed), UpToDate, Waltham, MA, 2006b.
• MIST II. A prospective, multicenter, randomized, double-blind, sham treatment controlled trial to evaluate the efficacy of patent foramen ovale closure with the BioSTAR® Bioabsorbable Septal Occlusion Device to prevent migraine headaches (http://www.pfo-migraine.com). 2006.
• Mortelmans K, Post M, Thijs V, Herroelen L, Budts W (2005). The influence of percutaneous atrial septal defect closure on the occurrence of migraine. Eur Heart J. 26(15):1533-7.
• Mugge A, Daniel WG, Angermann C, et al (1995). Atrial septal aneurysm in adult patients: a multicenter study using transthoracic and transesophageal echocardiography. Circulation. 91:2785-92.
• Overell JR, Bone I, Lees KR (2000). Interatrial septal abnormalities and stroke: a meta-analysis of case-control studies. Neurology. 55(8):1172-9.
• PREMIUM. Prospective Randomized Investigation to Evaluate Incidence of Headache Reduction in Subjects with Migraine and PFO Using the AMPLATZER® PFO Occluder Compared to Medical Management.
• http://www.premiumtrial.com/physician_info.html. 2006.
• Sadler TW (Septima Edicion). (1994). Langman. Embriologia medica. Medica Panamericana.
• Serena J (2006). Foramen oval permeable: ¿Cómo y de qué es fac-tor de riesgo? Neurología. 21(10):689-746
• Serena J, Segura T, Perez-Ayuso MJ, Bassaganyas J, Molins A, Davalos A (1998). The need to quantify right-to-left shunt in acute ischemic stroke: a case-control study. Stroke. 29(7):1322-8.
• Serena J, Martí Fàbregas J, Santamarina E, Rodríguez JJ, Pérez Ayuso MJ, Masjuan J, et al. Dávalos A for the CODICIA Study (2008). Recurrent stroke and massive right-to-left shunt: results from the prospective Spanish multicenter (CODICIA) study. Stroke; 39: 3131-6.
• Silver MD, Dorsey JS (1978). Aneurysms of the septum primum in adults. Arch Pathol Lab Med.102:62-5.
- 71128 lecturas